Nikola Čudina, Ena Oster, Hrvoje Pavasović, Andreja Prevendar Crnić, Frane Božić
Zavod za farmakologiju i toksikologiju, Veterinarski fakultet Sveučilišta u Zagrebu
 Izlaganje sa Međunarodnog znanstvenostručnog skupa
Izlaganje sa Međunarodnog znanstvenostručnog skupa
SažetakUvodFarmakokinetski i farmakodinamski profili antibiotikaKoncentracija prevencije mutanataProzor selekcije mutanataTrajanje antimikrobne terapijeSporootpuštujaće formulacije antibiotika i MWCStrategije suzbijanja antimikrobne rezistencijeOgraničenja i rizici nove paradigmeZaključakLiteraturaAbstract
Izvor: Zbornik radova 7. Hrvatski veterinarski kongres, Srebreno, 2024.
Sažetak
P osljednjih godina se u humanoj medicinskoj znanosti pojavila nova paradigma o razvoju antimikrobne rezistencije (eng. antimicrobial resistance, AMR) koja se zasniva na koncentraciji prevencije mutanata (eng., mutant prevention concentration, MPC) i prozoru selekcije mutanata (eng. mutant selection window, MSW). Koncentracija prevencije mutanata se definira kao ona koncentracija antibiotika koja inhibira rast najmanje osjetljivog mutanta prve generacije, a MSW se definira kao raspon koncentracija antibiotika između minimalne inhibitorne koncentracije (eng. minimum inhibitory concentration, MIC) i MPC-a pri kojemu dolazi do selektivnog pritiska i razvoja rezistentnih subpopulacija mikroorganizama. Iako su odgovarajuća istraživanja i primjena tih koncepata u humanoj medicini u porastu, vrlo je malo literaturnih podataka o njihovoj primjenjivosti u veterinarskoj medicini. Kako je AMR globalni problem u kontekstu koncepta „jednog zdravlja“, postoji potreba za zatvaranjem postojećeg jaza u literaturi. Koncept MSW-a nudi nova potencijalna rješenja za razvoj AMR-a u veterinarskoj medicini, ali njihova primjena nailazi na stanovite probleme i situacije što je indikator nužnosti razvijanja znanstvenog dijaloga u okviru navedenih novih spoznaja.
Ključne riječi: antimikrobna rezistencija, antibiotici, minimalna inhibitorna koncentracija, prozor selekcije mutanata, koncentracija prevencije mutanata
Uvod
Farmakokinetski i farmakodinamski profili antibiotika
Uz spomenuti MIC, važan farmakodinamski parametar antibiotika je minimalna baktericidna koncentracija (eng. minimum bactericidal concentration, MBC) koja predstavlja najnižu koncentraciju potrebnu da ubije 99.9% bakterijske populacije nakon izlaganja antibiotiku. Glavni farmakokinetski parametri antibiotika uključuju Cmax (vršna koncentracija lijeka u plazmi), AUC (površinu ispod krivulje odnosa koncentracije i vremena (eng. area under curve) i Tmax (vrijeme za koje lijek postigne Cmax). S obzirom na antimikrobnu aktivnost, antibiotici su svrstani u tri skupine: oni čije djelovanje ovisi o koncentraciji, oni čije djelovanje ovisi o vremenu te oni čije djelovanje ovisi o koncentraciji i vremenu (Toutain i sur., 2002). Obrasci aktivnosti sa odgovarajućim parametrima i primjerima antibiotika su prikazani u tablici 1.
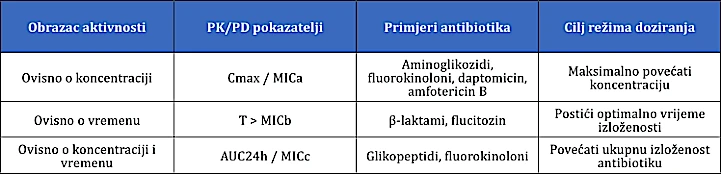
aOmjer vršne koncentracije lijeka u plazmi i minimalne inhibitorne koncentracije
bUkupno vrijeme u kojem je koncentracija lijeka u plazmi viša od minimalne inhibitorne koncentracije
cOmjer površine ispod krivulje odnosa koncentracije i vremena kroz 24 sata i minimalne inhibitorne koncentracije
Iako maksimalni terapijski učinak ovisi o koncentraciji na mjestu infekcije u organizmu, a minimalni toksični učinak o koncentraciji u neciljanim tkivima, koncentracije antibiotika u plazmi
su se pokazale najboljim parametrom za predviđanje kliničkog učinka lijeka (McKellar i sur., 2004.). Unatoč koristima navedenih parametara antibiotika, samostalno nisu dostatni za postizanje optimalnog režima doziranja u kontekstu borbe protiv razvoja AMR-e.
Koncentracija prevencije mutanata
Glavna zamjerka toj hipotezi je zanemarivanje eventualne prve generacije mutanata čija se MIC vrijednost u pravilu razlikuje od MIC-a izoliranog inokuluma iste bakterijske vrste.
Prilikom razvoja racionalnog režima doziranja, u obzir se uzimaju maksimalna učinkovitost antibiotika protiv nekog mikroorganizma te smanjivanje mogućnosti nastanka i selekcije rezistentnih mutanata. Kod korištenja isključivo MIC-a, problem pri ispunjavanju drugog uvjeta je veličina populacije mikroorganizma koja je, kao što je ranije spomenuto, u zaraženom organizmu značajno veća od in vitro inokuluma pri njegovom određivanju. Veliki broj bakterija u populaciji podrazumijeva njihovu visoku heterogenost, odnosno veću vjerojatnost postojanja prve generacije rezistentnih mutanata. U slučaju malog inokuluma „divljeg tipa“ bakterija (105 CFU (eng. colony forming units)) antibiotski tretman kojim se doseže MIC rezultirati će eradikacijom populacije dok izostanak tretmana antibioticima neće samostalno uzrokovati nastanak rezistentnih mutanata. U slučaju velikih inokuluma (108 CFU), antibiotskim tretmanom kojim se doseže MIC dolazi do eradikacije „divljeg tipa“ populacije, ali i mogućeg preživljavanja populacije postojećih mutanata na koju ta koncentracija antibiotika nije bila učinkovita. Učestali je i razvoj sekundarnih mutanata. Iz navedenog proizlazi zaključak da je unutar heterogenih velikih populacija mikroorganizama veća šansa postojanja rezistentnih mutanata pa koncentracije antibiotika na razini MIC-a često nisu dovoljne za ubijanje i tih rezistentnih mutanata.
To rezultira preživljavanjem i daljnjim razmnožavanjem rezistentne subpopulacije. Isto povećanje heterogenosti nastaje i progresijom infekcije u organizmu.
Za inhibiciju rasta mutanata prve generacije, uglavnom je potrebno postići koncentraciju antibiotika iznad vrijednosti MIC-a. Koncentracija antibiotika koja inhibira rast najmanje osjetljivog mutanta prve generacije naziva se koncentracijom prevencije mutanata (eng. mutant prevention concentration, MPC) (Canton i Morosini, 2011.).
Prozor selekcije mutanata

Paradigma prozora selekcije mutanata ukazuje na to da tradicionalno doziranje antibiotika iznad razine MIC-a, a ispod MPC-a ubija samo osjetljive bakterije te omogućava rast subpopulacije rezistentnih mutanata. Sukladno tome, doziranje antibiotika iznad MPC-a onemogućava preživljavanje mutanata (Zhao i Drlica 2002.; Zhao, 2003.; Drlica i Zhao, 2007.).
Trajanje antimikrobne terapije
Nadalje, u sažetku izvješća Svjetske zdravstvene organizacije (WHO) o uporabi osnovnih lijekova (2019.) navodi se da nedavne znanstvene spoznaje ukazuju na to da produžena uporaba antibiotika nakon povlačenja kliničkih znakova infekcije uzrokuje dodatni selektivni pritisak na širenje antimikrobne rezistencije. To je u skladu s ranijim istraživanjima u humanoj medicini koja dokazuju utjecaj produljene antimikrobne terapije amoksicilinom ili penicilinom na razvoj rezistencije kod komenzalne flore nazofarinksa (Guillemot i sur., 1998.; Schrag i sur., 2001). Shodno tome, istraživanje razvoja rezistencije bakterije Escherichia coli na kinolone pokazuje da se rezistentni sojevi nisu mogli otkriti prije 4. tjedna po završetku terapije ciprofloksacinom. Pojava rezistencije u tom razdoblju objašnjava se upravo padanjem koncentracije ciprofloksacina između 14. i 42. dana na razine unutar MSW-a, dok su prethodne visoke koncentracije bile iznad MPC vrijednosti (de Lastours i sur, 2012.).
Sporootpuštujaće formulacije antibiotika i MWC

Sporootpuštajuće formulacije zbog postupnijeg smanjivanja koncentracije lijeka u plazmi rezultiraju duljim održavanjem razina unutar raspona između MPC-a i MIC-a (Kastner i Guggenbichler, 2001.).
Strategije suzbijanja antimikrobne rezistencije
- održavanje doza iznad MPC-a,
- sužavanje MSW-a i
- „zatvaranje“ MSW-a uporabom dva kompatibilna antibiotika (Zhao i Drlica, 2001.).
Održavanje doza iznad MPC-a podrazumijeva brzo podizanje koncentracije antibiotika u plazmi iznad MPC-a, održavanje doza bez spuštanja ispod MPC-a te brzo spuštanje koncentracije u plazmi ispod MIC-a, dok je sužavanje MSW-a moguće odabirom antibiotika za koje je razlika između MPC-a i MIC-a manja nego kod drugih lijekova. Korištenje dva antibiotika u svrhu „zatvaranja prozora“ podrazumijeva njihovu sličnost u farmakokinetskim svojstvima kako bi oba lijeka istovremeno postigli MIC vrijednosti u plazmi. U takvoj situaciji, bakterijska populacija bi morala proći kroz dvije različite mutacije kako bi preživjela antibiotsku terapiju. Ova strategija je od velike koristi u situacijama kada je MPC vrijednost za određeni antibiotik iznad neškodljivih doza za određenu životinjsku vrstu što onemogućava doziranje iznad MPC (Wentzel i sur., 2022.). Pritom je bitno osigurati navedenu farmakokinetsku sličnost jer nepoklapanje farmakokinetskih parametara može rezultirati stvaranjem zasebnih MSW-a za svaki lijek, ako koncentracije jednog nisu iznad MIC-a dok je koncentracija drugog unutar svojeg MSW-a (Zhao i Drlica, 2001.). Prikaz takve farmakokinetske nekompatibilnosti i posljedice po „zatvorenost prozora“ nalazi se na slici 3.

Ograničenja i rizici nove paradigme
Zaključak
S obzirom na nedostatnost literaturnih podataka, kako bi održala korak s humanom medicinskom znanosti u cilju suzbijanja antimikrobne rezistencije, potreba za razvojem istraživanja o ovim predmetnim paradigmama u veterinarskoj znanosti je očigledna.
Literatura [… prikaži]
Nikola Čudina, Ena Oster, Hrvoje Pavasović, Andreja Prevendar Crnić, Frane Božić
STRATEGIES FOR COMBATING ANTIMICROBIAL RESISTANCE IN THE FRAMEWORK OF NEW PHARMACOKINETIC AND PHARMACODYNAMIC KNOWLEDGE
Abstract
I n recent years, a new paradigm has emerged in human medical science on the development of antimicrobial resistance (AMR), which is based on the mutant prevention concentration (MPC) and the mutant selection window (MSW). MPC is defined as the antibiotic concentration that inhibits the growth of the least sensitive first-generation mutant, while MSW is defined as the range of plasma antibiotic concentrations between the minimum inhibitory concentration (MIC) and the MPC at which selective pressure occurs and the development of resistant subpopulations of microorganisms. Although appropriate research and application of these concepts in human medicine is on the rise, there is very little literature on their applicability in veterinary medicine. As AMR is a global problem in the context of the “one health” concept, there is a need to close the existing gap in the literature. The concept of MSW offers new potential solutions for the development of AMR in veterinary medicine, but their application encounters problems and situations specific to veterinary medicine, which is an indicator of the necessity of developing a scientific dialogue within the framework of the aforementioned new knowledge.
Key words: antimicrobial resistance, antibiotics, minimum inhibitory concentration, mutant selection window, mutant prevention concentration


